Leczenie pacjentów chorych na szpiczaka mnogiego
Udostępnij
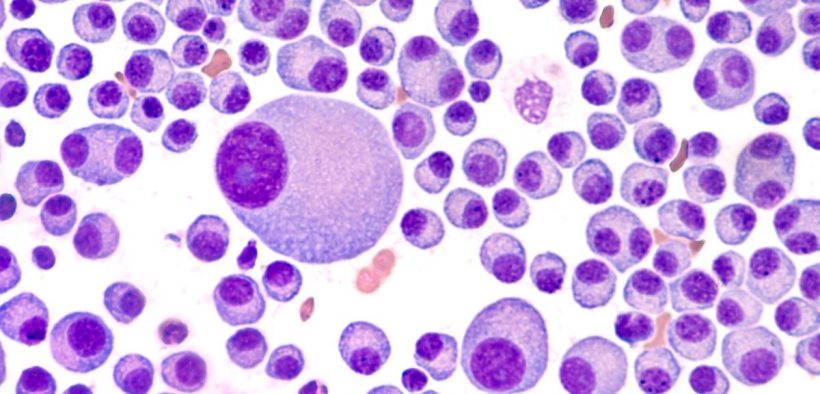
Szpiczak mnogi, MM (ang. Myeloma Multiplex), to rozsiany nowotwór złośliwy, który wywodzi się z monoklonalnych komórek plazmatycznych, odpowiadających za produkcje immunoglobulin oraz biorących udział w odpowiedzi humoralnej. Po kontakcie z antygenem plazmocyty osób chorujących na szpiczaka produkują immunoglobulinę tylko jednej klasy zamiast, jak u osób zdrowych, wszystkich klas. Zjawisko to nazywa się hipergammaglobulinemią poliklonalną [1, 2]. Szacuje się, że zachorowalność na MM w Europie wynosi 5,8/100 tys. osób, co stanowi 1-2% zachorowań na nowotwory i 10-15% nowotworowych schorzeń hematologicznych. W Polsce co roku rozpoznaje się ok. 1,5 tys. przypadków rocznie. Mediana wieku pacjenta w czasie rozpoznania to około 70 lat, a w 90% przypadków występuje powyżej 50. r.ż.. Stosunek liczby zachorowań mężczyzn do zachorowań kobiet wynosi 1,21 [2, 3, 4].
Rozpoznanie
Pierwszą oznaką choroby może być obecność białka monoklonalnego w moczu, która czasem powoduje postępujące upośledzenie sprawności nerek i ich uszkodzenie prowadzące do wystąpienia ostrej niewydolności [4].
Częstymi dolegliwościami zgłaszanymi przez pacjentów chorujących na MM są nasilające się, przewlekłe i oporne na leczenie bóle kostne występujące zwłaszcza w obrębie odcinka lędźwiowo-krzyżowego kręgosłupa, żeber, mostka i miednicy. Ból i skłonność do złamań, nawet przy niewielkim urazie bądź obciążeniu, wywołane są naciekaniem szpiku przez komórki plazmatyczne oraz wieloogniskowymi uszkodzeniami kości. Komórki szpiczaka wpływają na mikrośrodowisko szpiku zaburzając równowagę pomiędzy aktywnością osteoklastów i osteoblastów, co skutkuje wzmożoną resorpcją. Destrukcja kośćca dotyczy najczęściej szkieletu osiowego i u około 80% chorych ma postać ognisk osteolizy, czasem jednak pojawia się charakterystyczny obraz tkanki kostnej „wygryzionej przez mole”. Zdarza się, że pierwszym dostrzeżonym objawem jest złamanie wymagające pomocy ortopedy lub neurochirurga [2, 3, 4, 5].
Objawami MM są również: bladość skóry i spojówek spowodowane niedokrwistością, osłabienie, czasem utrata masy ciała, zmniejszenie wzrostu i zmiana sylwetki chorego (związane z uszkodzeniami kręgosłupa). Podejrzenie powinny również wzbudzić nawracające infekcje układu moczowego lub oddechowego [2, 3, 4, 5].
U około 30% pacjentów choroba ma charakter bezobjawowy i jest rozpoznawana po wykonaniu rutynowych badań kontrolnych i wykazaniu nieprawidłowości w wynikach laboratoryjnych (np. podwyższone OB, niedokrwistość czy białkomocz). Zgodnie z opracowanymi przez IMWG (ang. International Myeloma Working Group) kryteriami uszkodzenia narządowego (SliM CRAB – Tabela 1.), w przypadku występowania minimum jednego objawu wynikającego z klonalnego rozrostu plazmocytów rozpoznaje się szpiczaka plazmocytowego [2, 3, 4, 5].
Tabela 1. Zmodyfikowane kryteria narządowego uszkodzenia związanego ze szpiczakiem plazmocytowym (SLiM CRAB) [3].
| C (Calcium – wapń) | stężenie wapnia w surowicy > 0,25 mmol/l (>1 mg/dl) powyżej górnej granicy wartości referencyjnej lub >2,75 mmol/l (>11 mg/dl) |
| R (Renal Insufficiency– niewydolność nerek) | stężenie kreatyniny w surowicy >177 μmol/l (>2 mg/dl) lub klirens kreatyniny <40 ml/min (mierzony lub wyliczony) |
| A (Anemia – niedokrwistość) | stężenie hemoglobiny 2 g/dl poniżej dolnej wartości referencyjnej lub <10 g/dl |
| B (Bones – kości) | jedno lub więcej ognisk osteolitycznych w klasycznym badaniu radiologicznym, tomografii komputerowej (CT) lub badaniu pozytonowej tomografii emisyjnej (PET/CT) |
| S (Sixty – 60) | odsetek klonalnych plazmocytów w szpiku lub biopsji tkankowej co najmniej 60% |
| Li (Light Chains – łancuchy lekkie) | stosunek stężenia klonalnych do nieklonalnych (ang. involved/uninvolved) wolnych łańcuchów lekkich w surowicy, ocenianego metodą opartą na przeciwciałach poliklonalnych (Binding Site, UK) co najmniej 100, przy czym stężenie łańcucha klonalnego w surowicy (ang. involved) wynosi co najmniej 100 mg/l |
| M (Magnetic Resonanse – tomografia rezonansu magnetycznego) | obecność co najmniej dwóch ogniskowych nacieków w badaniu rezonansu kośćca o wymiarze co najmniej 5 mm każdy |
Klasyfikacja
Szpiczak mnogi może występować w kilku postaciach:
- Choroba występująca w jednym miejscu [3, 4]:
- Plazmocytoma – guz plazmocytowy kości lub poza nią. We krwi lub w moczu może zostać oznaczona niewielka ilość białka monoklonalnego, brak natomiast komórek nowotworowych w szpiku, a uszkodzenie kości jest ograniczone do obszaru guza. Postać ta może prowadzić do uogólnionego zajęcia szpiku [3, 4].
- Choroba rozsiana [3, 4]:
- Szpiczak mnogi wydzielający typu IgA lub IgG – występuje najczęściej. We krwi oznacza się podwyższone stężenie białka całkowitego, obecne jest białko monoklonalne IgA lub IgG (rzadko wydzielane są inne typy immunoglobulin).
- Szpiczak typu choroby łańcuchów lekkich – u około 20% chorych. Charakteryzuje go duża ilość białka w moczu i skłonność do uszkodzenia nerek. Białko monoklonalne typu łańcuchów lekkich jest trudne do oznaczenia w zwykłych badaniach krwi.
- Szpiczak mnogi niewydzielający – postać rzadko diagnozowana. W jej przebiegu brak jest białka monoklonalnego w moczu i we krwi, rzadziej obserwuje się hipergammaglobulinemię, hiperkalcemię i niewydolność nerek. Dochodzi natomiast do obniżenia stężenia całkowitego białka, ze względu na ograniczone wytwarzanie prawidłowo funkcjonujących białek odpornościowych.
- Pierwotna białaczka plazmatyczno-komórkowa – stanowi 2-5% zachorowań na szpiczaka. W rozmazie krwi obwodowej obecne są liczne zmienione nowotworowo plazmocyty. Odmiana bardziej agresywna od pozostałych, która może pojawiać się podczas przebiegu innych typów choroby [3, 4].
- Choroba bezobjawowa – szpiczak „tlący się” – wczesne bezobjawowe stadium kliniczne, w którym stwierdza się białko monoklonalne w moczu bądź krwi (mediana stężenia wynosi 3 g/dl), jednak niewiele jest komórek nowotworowych. Dotyczy ok. 8% pacjentów, zawartość plazmocytów w ich szpiku to ok. -10-20%. W stadium tym nie ma objawów uszkodzenia narządowego. Ryzyko progresji choroby do objawowej postaci szpiczaka wynosi 10% rocznie przez pierwsze 5 lat od postawienia diagnozy [3, 4].
U pacjentów, u których w trakcie diagnostyki wykrywa się obecność charakterystycznego białka monoklonalnego, jednak objawowi temu nie towarzyszą inne nieprawidłowości, stwierdza się obecność gammapatii monoklonalnej o nieustalonym znaczeniu. Występuje ona u 3-4% osób powyżej 50. r.ż., a ryzyko przejścia w szpiczaka wynosi ok. 1% rocznie, dlatego pacjenci są poddawani okresowym badaniom kontrolnym [3, 4].
Charakterystyka leków stosowanych w terapii
Leki immunomodulujące
Grupa substancji czynnych o podobnej strukturze chemicznej, do której należą: talidomid, lenalidomid i pomalidomid. Wpływają na mikrośrodowisko szpiku kostnego i komórki szpiczaka przez hamowanie angiogenezy, regulację aktywności cytokinm a także wzmocnienie funkcji i liczby komórek efektorowych układu immunologicznego (komórki NK, NK-T, limfocyty T). Oddziałują one również na zmiany kostne zwiększając aktywność osteoblastów i hamując różnicowanie osteoklastów [6, 7].
Talidomid zsyntetyzowano i wprowadzono do lecznictwa w 50. latach XX wieku. Początkowo był on stosowany jako środek nasenny, sedatywny i przeciwbólowy, a ze względu na właściwości przeciwwymiotne zalecano go w przypadku nudności u kobiet w pierwszym trymestrze ciąży. Z powodu działania teratogennego (niewykształcenie kończyn bądź ich zniekształcenie) lek wycofano z obrotu. Pomimo zaprzestania dystrybucji, badania nad mechanizmem działania były kontynuowane [8, 9].
W 1999 r. Sighal i wsp. opublikowali pracę na temat możliwości wykorzystania leku w terapii MM. Obecnie talidomid jest szeroko stosowany w tym schorzeniu w połączeniu z lekami o odmiennym mechanizmie działania [6, 7, 8, 9]. Badania, których celem było zmodyfikowanie cząsteczki talidomidu tak, aby zmniejszyć toksyczność, a zarazem zintensyfikować jego działanie, zaowocowały wprowadzeniem do obrotu analogów: lanalidomidu i pomalidomidu. Lenalidomid 2 tys. razy silniej stymuluje proliferację limfocytów T i wytwarzanie interleukiny-2 niż talidomid, jednocześnie rzadziej powoduje senność i polineuropatię.
Jest rekomendowany w terapii opornych i nawrotowych postaci MM. Pomalidomid to lek 10 razy silniejszy niż lenalidomid, którego dawka, w odróżnieniu od pozostałych substancji czynnych z tej grupy, nie musi być redukowana w przypadku niewydolności nerek. Jest wskazany w terapii chorych po zastosowaniu minimum dwóch linii leczenia, w tym schematami z lenalidomidem i bortezomibem [6, 7, 8, 9].
Inhibitory proteasomu
Proteasomy to układy wieloenzymatyczne, biorące udział w degradacji nieprawidłowych białek. Zmienione komórki nowotworowe są niestabilne genetycznie i wytwarzają duże ilości takich protein. Zahamowanie funkcji proteasomów powoduje nagromadzenie defektywnych białek w świetle retikulum plazmatycznego, prowadząc do apoptozy komórki [11]. Pierwszym lekiem z tej grupy wprowadzonym do terapii jest bortezomib, będący silnym, odwracalnym inhibitorem proteasomów.
Udowodniono, że cechuje go większa aktywność w stosunku do proliferujących komórek nowotworu niż do komórek prawidłowych. W wyniku przeprowadzonych badań klinicznych ustalono, że bortezomib wykazuje synergizm działania z innymi cytostatykami, uwrażliwiając komórki MM na ich działanie, dlatego zaleca się stosowanie go w schematach wielolekowych. Zaobserwowano również, że terapia jest skuteczna zarówno w pierwszej linii leczenia jak i w przypadku szpiczaka opornego lub nawrotowego.
Toksyczność bortezomibu w postaci trombocytopenii, polineuropatii, a także oporność stały się dla badaczy bodźcem do poszukiwania nowych cząsteczek o podobnym mechanizmie działania [10, 11]. Pierwszym inhibitorem proteasomów II generacji, zatwierdzonym przez FDA, jest karfilzomib. Lek ten ma działanie nieodwracalne i sprawdza się w terapii u świeżo zdiagnozowanych pacjentów, a także w przypadku nawrotów choroby.
Jego działanie przeciwnowotworowe jest podobne do działania bortezomibu, pokonuje jednak oporność na ten lek. Najczęstszymi objawami toksyczności są małopłytkowość i niedokrwistość, cechuje go jednak niski wskaźnik rozwoju neuropatii obwodowej [11, 12]. Iksazomib natomiast to pierwszy zarejestrowany lek z tej grupy, który jest podawany doustnie. Wiąże się on z proteasomem w sposób odwracalny i rzadziej niż bortezomib powoduje polineuropatię.
W badaniach klinicznych wykazano skuteczność w leczeniu chorych z nawrotowym szpiczakiem, którym dotychczas podawano kombinacje substancji o różnych mechanizmach działania, m.in. schematy z bortezomibem, lenalidomidem i deksametazonem. Niestety, obecnie nie jest refundowany w Polsce [11, 12, 13].
Przeciwciała monoklonalne
Jedynym refundowanym w ramach programu lekowego przeciwciałem monoklonalnym stosowanym w terapii MM jest daratumumab. Lek ten wiąże antygen CD-38 pośredniczący w przekazywaniu sygnałów do wnętrza komórki, regulacji procesów adhezji, zasiedlania i migracji. Udowodniono również, że indukuje on proliferację jednojądrzastych komórek krwi, produkcję interferonu γ oraz interleukiny 6. Antygen jest obecny w niewielkich ilościach na powierzchni komórek nabłonkowych, nerwowych, mięśniowych, mielo- i limfoidalnych.
Jego nadekspresję zaobserwowano na komórkach nowotworów limfoproliferacyjnych, m.in. MM. Łącząc się z antygenem CD-38 daratumumab indukuje układ dopełniacza i lizę komórki oraz cytotoksyczność zależną od przeciwciał, w której m.in. komórki naturalnej cytotoksyczności prowadzą do śmierci komórki przez wiązanie z fragmentem Fc przeciwciała. W badaniach wykazano także, że lek ten indukuje apoptozę i zanik aktywności enzymatycznej.
Jest on dobrze tolerowany przez pacjentów, zaobserwowano obecność reakcji związanych głównie z infuzją: nudności, kaszel i gorączkę, jednak ustępowały one po zastosowaniu glikokortykosteroidów, a ich natężenie malało w trakcie leczenia. Daratumumab cechuje się zaczną skutecznością zarówno w monoterapii, jak i w skojarzeniu z lekami o innych mechanizmach działania. W Polsce refundacji podlega leczenie tym przeciwciałem pacjentów z opornym lub nawrotowym MM w skojarzeniu z bortezomibem i deksametazonem.
Kolejnym lekiem zaaprobowanym przez FDA i EMA do terapii nawrotowego i opornego MM jest elotuzumab. Przeciwciało to jest skierowane przeciw glikoproteinie powierzchniowej CS1, znajdującej się na plazmocytach (prawidłowych i monoklonalnych), a także w niewielkich ilościach na limfocytach T i komórkach NK oraz w surowicy pacjentów z MM. Antygen zalicza się do rodziny cząsteczek powierzchniowych, SLAM (ang. Signaling Lymphocytic Activation Molecule), o właściwościach immunomodulujących.
Uważa się, że glikoproteina CS1 wpływa na rozwój limfocytów B, hamując zarazem limfocyty T, ponadto aktywuje komórki NK. Prawdopodobnie wspomaga ona również adhezję komórek, co może skutkować progresją MM. Elotuzumab działa głównie poprzez mechanizm cytotoksyczności komórkowej zależnej od przeciwciał przy udziale komórek NK. Wyniki badań sugerują niewielką rolę tego leku w monoterapii, natomiast obiecujące są doniesienia dotyczące efektu synergistycznego zastosowania w terapii skojarzonej z lekami immunomodulującymi i inhibitorami proteasomu.
Z uwagi na to, że glikoproteiny powierzchniowe, będące celem działania przeciwciał monoklonalnych, nie ulegają modyfikacjom z powodu mutacji i innych zmian cytogenetycznych w przebiegu choroby, wydaje się, że mogą one stanowić opcje terapeutyczną dla pacjentów z grup wysokiego ryzyka. Obecnie trwają liczne badania dotyczące możliwości zastosowania kolejnych leków należących do tej grupy w terapii MM [6, 14, 15].
Inhibitory deacetylazy histonowej
Panobinostat to jedyny lek z tej gruby zarejestrowany przez FDA i EMA w terapii nawrotowego lub opornego MM u pacjentów po wcześniejszej terapii bortezomibem i lekami immunomodulującymi. Podstawą rejestracji były badania, w których zastosowano lek w skojarzeniu z bortezomibem i deksametazonem, uzyskując znaczący wpływ na czas przeżycia pacjentów. Jego mechanizm działania polega na zahamowaniu deacetylazy histonowej, powodując kumulację acetylowanych histonów i innych białek, co skutkuje zatrzymaniem cyklu komórkowego lub apoptozą części zmienionych komórek.
Wykazuje on większą cytotoksyczność w stosunku do komórek nowotworowych niż prawidłowych. Do przerwania leczenia z powodu toksyczności, głównie w postaci zaburzeń pokarmowych, małopłytkowości i wydłużenia odstępu QT, dochodzi w ponad 50% przypadków, co znaczenie ogranicza jego zastosowanie kliniczne. Pomimo to, z uwagi na nowatorski mechanizm działania i doustną postać leku, ma on duży potencjał w terapii [4, 12, 16].
Leki alkilujące
Mechanizm działania leków polega na alkilacji nukleofilowych grup zasad pirymidynowych i purynowych, w wyniku której dochodzi do tworzenia nieprawidłowych połączeń zasad w trakcie syntezy DNA oraz rozluźnienie ich połączenia z resztą cukrową, co prowadzi do depurynacji skutkującej rozpadem DNA. Do leków z tej grupy, stosowanych w MM, należą: melfalan, cyklofosfamid i bendamustyna.
Przed pojawieniem się możliwości zastosowania w terapii mniej toksycznych substancji nowej generacji, tj. leków immunomodulujących, inhibitorów proteasomów i przeciwciał monoklonalnych, leki te, wraz z glikokortykosteroidami, były podstawą leczenia MM. Do dziś stanowią istotny element kombinacji z lekami o odmiennych mechanizmach działania [3, 10, 17].
Leczenie
Leczenie pierwszego rzutu
U pacjentów, u których na podstawie kryteriów SliM CRAB zdiagnozowano objawowego szpiczaka plazmocytowego, należy rozpocząć leczenie, którego celem jest indukcja remisji. Chorzy, których stan ogólny jest dobry, poniżej około siedemdziesiątego roku życia mogą zostać zakwalifikowani do leczenia mieloablacyjnego, związanego z nieodwracalnym uszkodzeniem szpiku kostnego chemioterapią wysokodawkową, HDT (ang. High-Dose Therapy), z towarzyszącym przeszczepem autologicznych komórek krwiotwórczych, autoHSCT (ang. auto hematopoietic stem cell transplantation).
Leczenie indukujące przebiega według protokołów VCD (bortezomib, cyklofosfamid, deksametazon), VTD (bortezomib, talidomid, deksametazon) albo PAD (bortezomid, doksorubicyna, deksametazon). Po 3-4 cyklach leczenia indukującego zazwyczaj przystępuje się do rozpoczęcia procedury pobrania komórek nazywanej mobilizacją, a następnie do przeszczepienia. Po autoHSCT stosuje się dodatkowe 2-3 cykle w pełnych lub zredukowanych dawkach (tzw. konsolidacja leczenia) [3, 10].
Pacjenci, którzy nie zostaną zakwalifikowani do przeszczepu, są poddani terapii bazującej na niewielkich dawkach melfalanu z dodatkiem talidomidu lub bortezomibu, czasem stosowane są też schematy VCD lub VTD [3, 10].
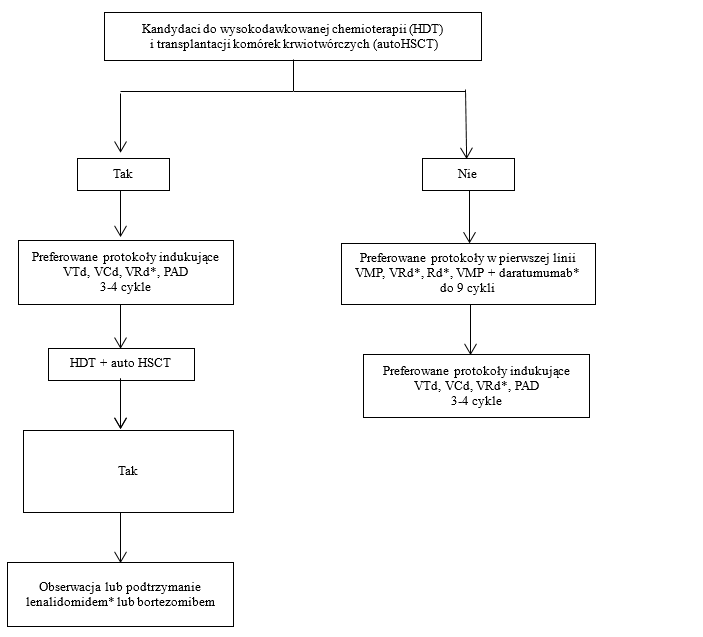
VTd – bortezomib, talidomid, deksametazon; VCd – bortezomib, cyklofosfamid, deksametazon; VRd* – bortezomib, lenalidomid, deksmaetazon; PAD – bortezomib, antracyklina, deksametazon; VMP – bortezomib, melfalan, prednizon; Rd* – lenalidomid, deksametazon; MPT – melfalan, prednizon, talidomid; MPR-R – melfalan, prednizon, lenalidomid; Vd – bortezomib, deksametazon; BP – bendamustyna, prednizon; CTd – cyklofosfamid, talidomid, deksametazon.
* Obecnie brak finansowania w Polsce.
Rysunek 1. Algorytm terapii u pacjentów z nowo rozpoznanym szpiczakiem plazmocytowym [3].
Leczenie podtrzymujące
Lekami stosowanymi jako terapia podtrzymująca odpowiedź u pacjentów z MM są: talidomid, bortezomib i lenalidomid (nierefundowany w tym wskazaniu w Polsce). Talidomid jest stosowany w dawce 50-100 mg dziennie p.o. u pacjentów bez niekorzystnych zmian genetycznych do momentu pojawienia się objawów toksyczności. Wykorzystanie bortezomibu ogranicza jego neurotoksyczność, zaletą jest natomiast możliwość podawania pacjentom z niewydolnością nerek oraz zagrożonych powikłaniami zakrzepowo-zatorowymi. Zazwyczaj w terapii podtrzymującej podaje się go w postaci cotygodniowej iniekcji podskórnej [3, 10].
Leczenie opornych na leczenie indukujące postaci szpiczaka
Brak nawet minimalnej odpowiedzi na wszelkie terapie nazywany jest pierwotną opornością na leczenie. Problem ten może dotyczyć zarówno osób, których stan stale się pogarsza, jak i pacjentów bez klinicznych objawów progresji. Gdy stan pacjenta jest stabilny, nie wymaga on intensyfikacji leczenia, lecz uważnej obserwacji. Osoby, u których choroba postępuje, warto kwalifikować do udziału w badaniach klinicznych, umożliwiających stosowanie nowoczesnych terapii nierefundowanych w Polsce, np. iksazomibem, elotuzumabem czy panobinostatem.
U pacjentów, których stan zdrowia pozwala na zastosowanie HDT wraz z autoHSCT, można również rozważyć ten rodzaj leczenia, gdyż częstość uzyskanych odpowiedzi w przypadku oporności pierwotnej to ok. 70%. Przed HDT stosuje się leczenie cytoredukujące, uwzględniając toksyczność poprzedniej linii leczenia. Jeśli dotychczas był stosowany schemat z talidomidem, można zmienić go na kombinację leków z bortezomibem.
Gdy mamy do czynienia ze szczególnie agresywną postacią MM, u pacjentów nieleczonych talidomidem warto wziąć pod uwagę podawanie go łącznie z lekiem sterydowym, cisplatyną, doksorubicyną, etopozydem i cyklofosfamidem lub stosowanie schematów opartych na związkach platyny. U chorych z zaawansowaną polineuropatią wskazany jest lenalidomid [3].
Pacjentom niekwalifikującym się do HDT, opornym lub źle tolerującym talidomid, u których w pierwszej linii zastosowano CTD, zaleca się układ oparty na bortezomibie, np. VMP. Natomiast gdy w leczeniu indukującym zastosowano VMP i występuje zaawansowana polineuropatia, wskazane jest zastosowanie schematu z lenalidomidem lub bendamustyną.
W przypadku pacjentów, u których dotychczas zastosowano zarówno kombinację z bortezomibem, jak i lenalidomidem, warto rozważyć terapię pomalidomidem z dodatkiem deksametazonu i np. cyklofosfamidu. Alternatywą są refundowane od 1.07.2019 r. w ramach programu lekowego: daratumumab stosowany z bortezomibem i deksametazonem uraz karfilzomib w skojarzeniu z lenalidomidem i deksametazonem [3].
Leczenie nawrotowych postaci szpiczaka
Szpiczak plazmocytowy jest chorobą nieuleczalną i ma charakter nawrotowy, a czas odpowiedzi na zastosowane leczenie przy każdym kolejnym nawrocie jest coraz krótszy. W wyniku terapii usunięte zostają klony lekowrażliwe, pozostają jednak odmiany agresywne ze skumulowanymi abberacjami genetycznymi. Konieczne jest zatem jak najwcześniejsze włączenie terapii wielolekowych, skutecznych wobec różnorodnych klonów MM.
Zgodnie z zaleceniami, jeśli do nawrotu choroby doszło po ok. 20-24 miesiącach, wskazane jest powtórzenie schematu początkowego, natomiast jeśli remisja była krótsza niż 9-12 miesięcy, należy dobrać terapię alternatywną. W celu uzyskania odpowiedzi i wydłużenia czasu wolnego od progresji zaleca się łączenie nowoczesnych leków z tradycyjnymi cytostatykami. Podanie kombinacji dwóch leków (bortezomib, talidomid, pomalidomid, lenalidomid w połączeniu z cytostatykiem lub deksametazonem) daje całkowity odsetek odpowiedzi ok. 41-61%.
Zgodnie z uzyskanymi dotychczas wynikami badań, zastosowanie w terapii trzech lub czterech leków (cytostatyku, deksametazonu, inhibitora proteasomów i leku immunomodulującego) ma większą skuteczność. Obiecujące są również analizy dotyczące leczenia przeciwciałami monoklonalnymi – elotuzumabem i daratumumabem. Aby ograniczyć występowanie działań niepożądanych po stabilizacji stanu zdrowia można zastanowić się nad przerwaniem stosowania leków alkilujących lub bortezomibu, a leki immunomodulujące mogą być stosowane do progresji bądź pojawienia się znacznej toksyczności.
Pacjentów, u których w wyniku poprzedniej transplantacji uzyskano remisję trwającą minimum 18-24 miesięcy, można ponownie zakwalifikować do terapii HDT wraz z autoHSCT. Gdy poprzednie leczenie z autoHSCT było nieskuteczne lub u chorego występują wskaźniki wysokiego ryzyka, a stan biologiczny na to pozwala, warto wziąć pod uwagę przeszczepienie allogenicznych komórek macierzystych (alloHSCT).
Jest to jedyna metoda, która daje szanse wyleczenia, jednakże z uwagi na dużą śmiertelność i zagrożenie wystąpienia reakcji „przeszczep przeciwko gospodarzowi” jest wykonywana rzadko. Jeśli szpiczak ma charakter miejscowy, można zastosować radioterapię, ograniczając tym samym toksyczność i zachowując więcej opcji w przypadku uogólnionego nawrotu [3, 6].
Terapia osób starszych
Około 28% chorych na MM stanowią osoby w wieku 65-74 lata, a 37% pacjenci po 75. r.ż. W terapii osób starszych należy zwrócić szczególną uwagę na stan zdrowia (zwłaszcza zmniejszenie wydolności narządów), choroby współistniejące, sprawność ruchową i polifarmakoterapię. Jeśli jest to możliwe, zaleca się również, by leczenie było prowadzone we współpracy z lekarzem geriatrą.
Głównym celem w tej grupie chorych jest osiągnięcie jak najdłuższego czasu całkowitego przeżycia przy równoczesnym zapewnieniu jak najlepszej jakości życia. Udowodniono, że zobiektywizowany przez ocenę geriatryczną stan biologiczny jest czynnikiem prognostycznym niezależnym od stopnia zaawansowania MM.
W przypadku pacjentów powyżej 75. r.ż. bądź takich, u których występują choroby współistniejące wraz z niewydolnością narządów, wskazana jest indywidualizacja leczenia przez zmniejszenie dawek stosowanych leków. Zastosowanie zbyt obciążającego schematu może skutkować wystąpieniem powikłań i przerwaniem leczenia [3, 18].
Pacjenci z niewydolnością nerek
Niewydolność nerek (NN) dotyka około połowy pacjentów chorujących na MM; jest to jeden z czynników determinujących krótszy czas przeżycia. Zgodnie z doniesieniami naukowymi przywrócenie ich funkcji sprawia, że rokowanie jest zbliżone do pacjentów bez NN. Podstawą leczenia tej grupy pacjentów jest leczenie MM, gdyż szybkie rozpoczęcie terapii przeciwszpiczakowej jest istotnym elementem poprawy stanu narządu. Warto również pamiętać o konieczności odpowiedniego nawodnienia. Badania prowadzone z udziałem chorych z NN wykazały skuteczność stosowania schematów leczenia opartych na bortezomibie (np. połączenie z melfalanem lub bendamustyną), którego okres półtrwania jest niezależny od przesączania nerkowego. W przypadku gdy nie można zastosowań bortezomibu, zaleca się podawanie talidomidu, lenalidomidu lub pomalidomidu. Podczas stosowania lenalidomidu konieczne jest dostosowanie dawki opartej na klirensie kreatyniny. Udowodniono również, że równoczesne zastosowanie bortezomibu i lenalidomidu lub talidomidu z wysokimi dawkami deksametazonu pozwalało na uzyskanie krótszego czasu odpowiedzi nerkowej. HDT wraz z auto-HSCT nie są przeciwwskazane u chorych z NN – również u pacjentów dializowanych. Zaburzenia te nie wpływają na proces mobilizacji komórek i ich wszczepienie, jednakże wykazano większe ryzyko powikłań zwłaszcza ze strony przewodu pokarmowego oraz zwiększoną śmiertelność (>4% u pacjentów z NN w porównaniu z <1% u chorych bez NN) [3, 19, 20].
Zakończenie
Starzenie się społeczeństwa stawia przed nami nowe wyzwania, do których należy wzrost zapotrzebowania na leczenie pacjentów z chorobami, takimi jak MM, który występuje przeważnie u osób w podeszłym wieku. Dlatego niezwykle istotne jest systematyczne wykonywanie badań profilaktycznych, gdyż wczesne zdiagnozowanie i podjęcie leczenia przedłuża życie i poprawia jego jakość przez ograniczenie wystąpienia powikłań narządowych. Chociaż MM jest uznawany za chorobę nieuleczalną, wprowadzenie kolejnych substancji czynnych o różnych mechanizmach działania przekłada się na znaczącą poprawę rokowania [21, 22].
Autor:
mgr farm. Monika Malczewska
Praca poglądowa w ramach specjalizacji z farmacji klinicznej
Artykuł pochodzi z 51. Wydania kwartalnika „Farmakoekonomika Szpitalna”
Źródła:
- Mess E., Ornat M., Klaszczyk T., Olszewska-Szopa M., Usnarska-Zubkiewicz L.: Ocena jakości życia chorych na szpiczaka mnogiego – raport wstępny. Medycyna paliatywna 2018; 10(4): 208-215.
- Jagannath S., Richardson P., Munshi N. Szpiczak plazmocytowy i inne dyskrazje plazmocytarne. Nowotwory złośliwe. Postępowanie wielodyscyplinarne. Tom II. Czelej, 2012, 541-552.
- Giannopoulos K., Jamroziak K., Usnarska-Zubkiewicz L., Dytfeld D., Jurczyszyn A., Walewski J., Lech-Marańda E., Walter-Croneck A., Pieńkowska-Grela B., Wrobel T., Charliński G., Jędrzejczak W., Małkowski B., Druzd-Sitek A., Robak T., Mańko J., Giebel S., Czepko R., Meder J., Dmoszyńska A.: Zalecenia Polskiej Grupy Szpiczakowej dotyczące rozpoznawania i leczenia szpiczaka plazmocytowego oraz innych dyskrazji plazmocytowych na rok 2018/ Acta Haematologica Polonica. 2018; 49(4): 157-206.
- Polska Grupa Szpiczakowa. https://hematoonkologia.pl/polska-grupa-szpiczakowa. (stan z dnia 20.04.2020 r.).
- Michalak S., Rupa-Matysek J., Gil L.: Pacjent ze szpiczakiem plazmocytowym
w gabinecie lekarza rodzinnego. Rodz. 2016: 19(3): 152-157. - Jurczyszyn A., Olszewska-Szopa M.: Rola immunoterapii w leczeniu szpiczaka plazmocytowego. Prz. Lek.2016: 73(9): 659-665.
- Dmoszyńska A.: Leki immunomodulujące w terapii szpiczaka plazmocytowego. Onkol. Dypl. 2017:14(3): 17-22.
- Stępień A., Jamroziak K.: Cereblon: molekularny cel leków immunomodulujących. Acta Haematol. Pol. 2013: 44(3): 200-207.
- Pach K.: Talidomid i jego analogi- zastosowanie we współczesnej terapii. Farm. Pol. 2014: 70(10): 548-551.
- Jurczyszyn A., Grząśko N., Zacha J.: Dwu-, trzy- i czterolekowe schematy w leczeniu pierwszoliniowym szpiczaka plazmocytowego z uwzględnieniem efektów terapii
z zastosowaniem bortezomibu. Acta Haematol. Pol. 2014: 45(1): 26-34. - Romaniuk W., Ołdziej A., Zińczuk J., Kłoczko J.: Inhibitory proteasomów w terapii onkologicznej. Postępy Hig Med Dosw (online). 2015: 69: 1443-1450.
- Jurczyszyn A., Olszewska-Szopa M.: Najnowsze osiągnięcia w zakresie diagnostyki i leczenia szpiczaka plazmocytowego. Prz. Lek. 2017:74(1): 30-36.
- Giannopoulos K., Jędrzejczak W., Jamroziak K., Dytfeld D., Robak T., Hellman A.: Iksazomib u chorych z nawrotowym lub opornym na leczenie szpiczakiem plazmocytowym. Acta Haematol. Pol. 2017: 48(3): 160-164.
- Salomon- Perzyński A., Jamroziak K.: Rola daratumumabu w leczeniu chorych na nawrotowego i opornego szpiczaka plazmocytowego. Hematologia 2017: 8(4): 255-264.
- Olszewska-Szopa M., Jurczyszyn A.: Monoklonalne przeciwciała w szpiczaku plazmocytowym- przełom w terapii. Acta Haematol. Pol. 2015: 46(5): 359-366.
- Lipska K., Filip A., Gumieniczek A.: Postępy w badaniach nad inhibitorami deacetylaz histonów jako lekami przeciwnowotworowymi. Postępy Hig Med Dosw (online). 2018: 72: 1018-1031.
- Cegieła U., Janiec W., Pytlik M.: Leki stosowane w leczeniu nowotworów. Kompendium farmakologii. PZWL 2015: 508-512
- Jamroziak K.: Postępy w diagnostyce i leczeniu chorych na szpiczaka plazmocytowego. Hematologia 2015: 6(1): 10-18.
- Skwierawska K., Waszczuk-Gajda A., Basak G.: Postępowanie w szpiczaku plazmocytowym z towarzyszącą niewydolnością nerek. Dypl. 2017: 14(2): 12-22
- Grosicki S.: Szpiczak plazmocytowy z niewydolnością nerek jako wyzwanie terapeutyczne. Acta Haematol. Pol. 2015: 46(2): 80-85.
- Giannopoulos K., Dwilewicz-Trojaczek J., Stompór T., Ligocki P., Stopiński M., Sutkowski M., Grząśko N., Morawska M., Kordecka A., Kordecka A., Kordecki M., Jurczyszyn A., Dytfeld D., Wróbel T., Jamroziak K., Druzd-Sitek A., Walter-Croneck A., Dmoszyńska A.: Wyzwania wczesnej diagnostyki szpiczaka plazmocytowego -algorytm diagnostyczny. Acta Haematol. Pol. 2019: 50(3): 121-129.
- Szymczyk A., Hus I.: Strategie optymalizacji terapii lenalidomidem u chorych na szpiczaka plazmocytowego. Acta Haematol. Pol. 2017: 48(4): 282-290.


