Leczenie żywieniowe nieodłączną częścią terapii chorób nowotworowych
Udostępnij

Leczenie żywieniowe stanowi nieodłączny element holistycznej terapii chorób nowotworowych. Obecnie pojawia się coraz więcej badań potwierdzających skuteczność stosowania immunożywienia w grupie pacjentów onkologicznych. Pacjenci onkologiczni, z powodu częstych zaburzeń wchłaniania, wymagają indywidualnej interwencji żywieniowej, która poprawia wskaźniki stanu odżywienia oraz przeciwdziała pogłębianiu się niedoborów. W niniejszej pracy dokonano przeglądu doustnych suplementów pokarmowych (ONS, ang. Oral Nutritional Supplements), uwzględniając ich podział na preparaty kompletne, niekompletne i wysokobiałkowe. Stosowanie ONS może mieć pozytywny wpływ na stan kliniczny chorego i przyczyniać się do poprawy jakości jego życia. Preparaty ONS charakteryzuje uniwersalność, dostępność oraz łatwość w użyciu. Szeroka oferta handlowa pozwala kadrze medycznej precyzyjnie dostosować preparat do potrzeb pacjenta.
Leczenie żywieniowe
Pacjenci onkologiczni, ze względu na liczne zaburzenia wchłaniania, znaczną utratę masy ciała, zwiększone zapotrzebowanie na makro- i mikroskładniki diety, wymagają indywidualnego planu leczenia żywieniowego. Wszystkie procedury dążące do poprawy stanu odżywienia mają istotny wpływ na czas i jakość życia pacjenta [1].
Prawidłowa interwencja żywieniowa (żywienie kliniczne) obejmuje następujące składowe [5]:
- ocenę stanu odżywienia,
- ocenę rodzaju i stanu nasilenia zaburzeń,
- określenie zapotrzebowania na składniki odżywcze,
- wybór drogi podaży (doustna, dojelitowa, dożylna lub mieszana),
- opracowanie planu żywienia,
- monitorowanie pacjenta i ocenę leczenia.
Żywienie drogą przewodu pokarmowego (żywienie dojelitowe/enteralne, ang. enteral nutrition) jest metodą pierwszego wyboru.
W przypadku możliwości stosowania żywienia drogą doustną, po konsultacji dietetycznej należy rozważyć [5]:
- fortyfikację diety kuchennej,
- wykorzystanie przemysłowych płynnych diet doustnych (ang. sip feeding).
Doustne suplementy pokarmowe
Doustne suplementy pokarmowe (ONS, ang. Oral Nutritional Supplements), znane również jako doustne płynne diety przemysłowe (ang. sip feeding), zgodnie z ustawą z dn. 25.08.2006 r. o bezpieczeństwie żywności i żywienia zostały określone jako suplementy diety. Zgodnie z definicją suplement diety jest to środek spożywczy będący skoncentrowanym źródłem witamin i składników mineralnych, wykazujący efekt odżywczy lub fizjologiczny [15]. Suplementy diety są wprowadzane do obrotu w formie umożliwiającej ich dawkowanie, najczęściej w postaci: kapsułek, tabletek, drażetek z proszkiem, ampułek z płynem, butelek z kroplomierzem. Są one przeznaczone do spożywania w małych, odmierzonych ilościach jednostkowych, z wyłączeniem substancji mających właściwości produktu leczniczego w rozumieniu przepisów Prawa farmaceutycznego [1]. Obwieszenie Ministra Zdrowia z dn. 16.06.2015 r. wprowadziło do obrotu ONS pod nazwą dietetyczny środek spożywczy specjalnego przeznaczenia medycznego [16].
Wytyczne międzynarodowe określają sytuacje wymagające interwencji żywieniowej w postaci doustnych suplementów pokarmowych:
- U dorosłych z niedożywieniem, definiowanym jako (spełnienie jednego z kryteriów) [5]:
– wskaźnik masy działa (BMI, ang. body mass index) poniżej 18,5 kg/m2,
– niezamierzona utrata masy ciała powyżej 10% (bez względu na czas) lub powyżej 5% w ciągu 3 miesięcy,
– BMI poniżej 20 kg/m2 oraz niezamierzona utrata masy ciała powyżej 5% w ciągu 3-6 miesięcy.
- U dorosłych z ryzykiem niedożywienia, definiowanym jako [5]:
– zmniejszone spożycie doustne lub zaprzestanie przyjmowania pokarmów przez więcej niż 5 dni lub/i w przypadku dużego prawdopodobieństwa zmniejszenia albo zaprzestania przyjmowania pokarmów przez 5 dni lub dłużej,
– zmniejszona absorpcja i/lub zwiększone zapotrzebowanie, i/lub zwiększona utrata składników odżywczych w przebiegu choroby,
– nasilone procesy kataboliczne.
Europejskie Towarzystwo Żywienia Klinicznego i Metabolizmu (ESPEN, ang. European Society for Clinical Nutrition and Metabolism) wskazuje dodatkowe warianty zastosowania leczenia żywieniowego:
- w okresie przedoperacyjnym u chorych z ryzykiem niedożywienia – włączenie interwencji żywieniowej na 10-14 dni, nawet kosztem odroczenia zabiegu,
- przedoperacyjne zastosowanie ONS bogatych w składniki immunomodulujące przez 5-7 dni u pacjentów onkologicznych, którzy oczekują na duże zabiegi operacyjne w obrębie przewodu pokarmowego.
Doustne suplementy pokarmowe występują w wersjach kompletnych pod względem składu (dostarczają wszystkich makro- i mikroskładników) lub w wersjach niekompletnych (wyselekcjonowanych). Osoby sprawujące opiekę nad leczeniem żywieniowym chorego powinny dołożyć wszelkich starań, aby plan fortyfikacji żywieniowej był dostosowany do indywidualnych potrzeb pacjenta. Powstały preparaty przeznaczone dla pacjentów z określonymi jednostkami chorobowymi, takimi jak: cukrzyca, niewydolność nerek czy choroby wątroby.
Preparaty niekompletne
Preparaty jednoskładnikowe stanowią dodatkowe źródło podaży energii lub makroskładników. Wyróżniamy preparaty:
1. Białkowe
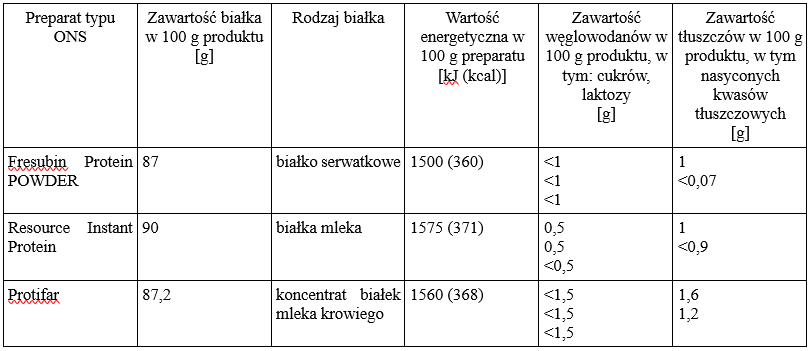
Nasilone procesy kataboliczne powodują zwiększoną utratę białka. Podaż białka dla chorego onkologicznego powinna wynosić 1,2-2 g/kg masy ciała/dobę [1]. Dostępne na rynku preparaty są dystrybuowane w formie proszku o neutralnym smaku, który rozpuszcza się w płynach lub dodaje do gotowych potraw. Są to preparaty o nieznacznej zawartości tłuszczów i węglowodanów, bezresztkowe, o niskiej zawartości laktozy.
Tabela 1. Charakterystyka preparatów białkowych typu ONS. Opracowanie własne
2. WęglowodanoweW przypadku pacjentów z chorobą nowotworową wykorzystywanie preparatów opartych na białkach serwatkowych wydaje się przynosić większe korzyści. W stosunku do kazeiny charakteryzuje je większa strawność, mniejsze ryzyko powikłań ze strony układu pokarmowego (takich jak wzdęcia, nudności i biegunka), ponadto u chorego szybciej pojawia się uczucie sytości [2].
Rynek doustnych suplementów pokarmowych proponuje jeden preparat oparty na maltodekstrynach – Faltomalt. Występuje on w postaci proszku do wymieszania z pokarmem lub napojem. Jest przeznaczony dla chorych wymagających uzupełnienia podaży energii. Jedna miarka – 5 g proszku – dostarcza 19 kcal. W 100 g preparatu znajduje się 96 g węglowodanów w postaci maltodekstryny. Preparat nie zawiera laktozy ani glutenu.
3. Tłuszczowe
Preparaty tłuszczowe stosuje się u pacjentów wymagających uzupełnienia podaży energii. Emulsja tłuszczowa – Calogen® – jest źródłem jedno- i wielonienasyconych kwasów tłuszczowych. Tłuszcze zastosowane w preparacie są pochodzenia roślinnego – na bazie oleju rzepakowego oraz słonecznikowego. Zawartość tłuszczów w 100 ml produktu wynosi 50 g.
4. Inne
Preparat dostępny pod nazwą Glutamine Plus® zawiera 4,6 g endogennego aminokwasu glutaminy w 100 g proszku i jest przeznaczony do rozpuszczania w płynach. Jest on wzbogacony o związki przeciwutleniające, takie jak: cynk, selen, witaminy E i C oraz β-karoten.
Badania nad metabolizmem glutaminy wskazują na jej wysoki obrót przez błonę śluzową przewodu pokarmowego, wątrobę, ośrodkowy układ nerwowy i komórki odpornościowe [2]. W trakcie choroby nowotworowej stężenie glutaminy w organizmie chorego spada, jednak nie wiadomo, co jest wynikiem niedoboru [3]. Zaobserwowano korzystny wpływ doustnej suplementacji glutaminy w przypadku zapalenia błony śluzowej, biegunek i wymiotów, będących częstym powikłaniem chemioterapii.
Jednak według ekspertów ESPEN nie ma wystarczających dowodów dotyczących terapeutycznego zastosowania glutaminy [4].
Preparaty kompletne
Doustne diety przemysłowe w swoim składzie zawierają białko, tłuszcze, węglowodany, witaminy, mikroelementy oraz wodę. Kompletność składu pozwala uzupełnić niedostateczną podaż energii i składników mineralnych w diecie chorego lub całkowicie ją zastąpić.
Doustne suplementy pokarmowe można klasyfikować w zależności od:
- gęstości energetycznej,
- zawartości białka,
- stopnia hydrolizy białka,
- jednostki chorobowej.
Jednakże wśród pacjentów onkologicznych każdy rodzaj preparatu może znaleźć zastosowanie, w zależności od indywidualnych potrzeb pacjenta [5].
Zgodnie z wytycznymi ESPEN [4] oraz POLSPEN [6], podaż energii określa się na poziomie 25-30 kcal/kg mc./dobę. Wśród pacjentów o prawidłowej masie ciała przeliczenia dokonuje się na podstawie aktualnej masy ciała, natomiast w przypadku pacjentów otyłych należy określić ich idealną masę ciała.
Pod względem gęstości energetycznej wyróżnia się preparaty:
- hipokaloryczne 0,5-0,9 kcal/ml diety;
- izokaloryczne 1-1,2 kcal/ml diety;
- hiperkaloryczne 1,3-2,4 kcal/ml diety.
W badaniu przeprowadzonym przez grupę z Lundholm, około 50% wszystkich pacjentów onkologicznych, u których zaobserwowano spadek masy ciała, było hipermetabolicznych w porównaniu z grupą kontrolną. Szereg prac wskazuje jednak na duże rozbieżności w podstawowej przemianie materii w zależności od rodzaju i lokalizacji nowotworu [4, 7].
Najczęściej stosowane są preparaty izokaloryczne, standardowe, np. Diasip® (1 kcal/1 ml).
Do produktów o wysokiej gęstości odżywczej należą: Nutridrink® (2,4 kcal/1 ml), Resource 2.0® (2 kcal/1 ml), Ensure Plus® (1,5 kcal/1 ml), ImpactOral® (1,44 kcal/1 ml), Fresubin Energy DRINK® (1,5 kcal/1 ml).
Preparaty wysokobiałkowe
Z przeglądu literatury wynika, że dawka aminokwasów zdolnych do utrzymania dodatniego bilansu białek u pacjentów z nowotworem może być bliska 2 g/kg/dzień [8]. Jest to zgodne z badaniem Wintera i wsp., którzy wykazali, że u pacjentów ze średnio zaawansowaną chorobą nowotworową występuje znaczna insulinooporność, w tym upośledzone wykorzystanie glukozy oraz zaburzenie anabolizmu białek w całym organizmie. Zwiększona podaż białka może przywrócić prawidłową anaboliczną odpowiedź białkową [9].
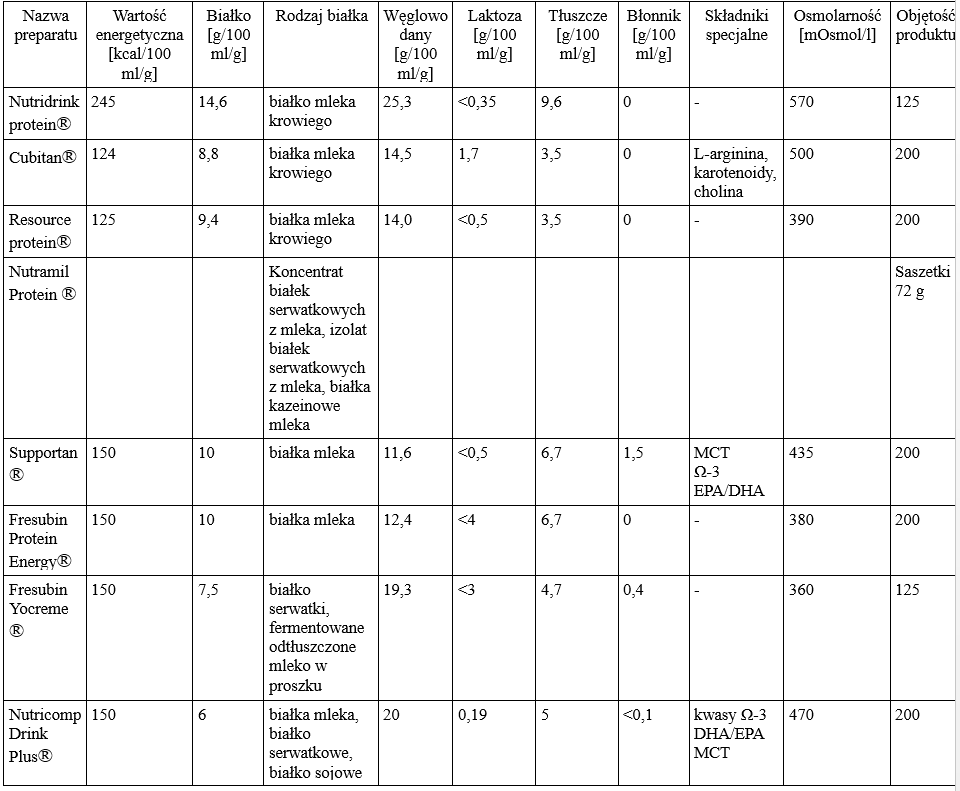
Tabela 2. Charakterystyka preparatów wysokobiałkowych. Opracowanie własne
Supportan® – 1,5 g błonnika/100 ml,Produkty bogatoresztkowe usprawniają perystaltykę jelit i regulują rytm wypróżnień. Znajdują szerokie zastosowanie w eliminowaniu powikłań leczenia, takich jak biegunki czy zaparcia. Wyróżnia się kilka produktów zawierających błonnik:
- Fresubin Yocreme® – 0,4 g błonnika/100 ml,
- Nutridrink Multi Fibre® – 3,6 g błonnika/100 ml,
- Fresubin Fibre Energy DRINK® – 2 g błonnika/100 ml,
- Forticare® – 2,1 g błonnika/100 ml,
- Diben Drink® – 2 g błonnika/100 ml.
Diety zawierające składniki immunostymulacyjne znajdują zastosowanie u chorych niedożywionych lub poddawanych rozległym operacjom. Olej rybny (najczęściej stosowane dawki: 4-6 g/dzień) oraz długołańcuchowe kwasy tłuszczowe N-3 (1-2 g/dzień) zmniejszają odpowiedź zapalną u pacjentów onkologicznych, o czym świadczy spadek wskaźników stanu zapalnego (IL 6 lub białko C-reaktywne) i spoczynkowy wydatek energetyczny [10]. Fearon i wsp. w randomizowanym badaniu klinicznym przedstawili zależności między dawkami kwasów tłuszczowych N-3 u pacjentów w grupie leczonej. Dane te sugerują, że do uzyskania korzyści klinicznych w punktach końcowych związanych z odżywianiem wymagane jest co najmniej 2 g/dobę [11].
W przypadku pacjentów onkologicznych należałoby rozważyć suplementację preparatami:
- Forticare® – wielonienasycone kwasy tłuszczowe 2,7 g, EPA – 601 mg, DHA – 298 mg/100 ml produktu;
- OralImpact® – kwasy tłuszczowe wielonienasycone 1,3 g, Ω – 3,6 g (w tym: EPA+DHA – 500 mg);
- Supportan DRINK® – EPA – 500 mg, DHA – 210 mg;
- Souvenaid® – wielonienasycone kwasy tłuszczowe 1,8 g, EPA – 240 mg, DHA – 960 mg.
Producenci doustnych suplementów pokarmowych kierują swoją ofertę – preparaty o odpowiednio zmodyfikowanym składzie – również do chorych z cukrzycą, zaburzeniem funkcji nerek czy niewydolnością wątroby.
Należy również zaznaczyć, iż każdy z wymienionych preparatów jest dostępny w wielu smakach, co umożliwia choremu wybór dostosowany do własnej preferencji smakowej.
Zalety i wady stosowania doustnych suplementów pokarmowych
Przegląd publikacji naukowych na temat skuteczności ONS u pacjentów onkologicznych w stanie kacheksji, wykonany przez Jin-Min Kim i Mi-Kyung Sung, sugeruje, że interwencja żywieniowa poprawia wskaźniki stanu odżywienia, stanu zapalnego, funkcji układu odpornościowego i polepsza standard życia chorych. Istnieją dowody na to, iż u pacjentów poddanych (adiuwantywnej) radioterapii wsparcie żywieniowe poprawia niektóre aspekty jakości życia [12, 13].
Zdecydowaną zaletą preparatów typu ONS jest skoncentrowanie składników odżywczych i energii w niewielkiej objętości. Ze względu na ich jałowość, mogą być proponowane pacjentom w stanie immunosupresji. Gotowość do użycia, uniwersalność i dostępność przepisów przygotowanych przez producentów ułatwia ich stosowanie. Szeroka oferta handlowa pozwala kadrze medycznej precyzyjnie dostosować preparat do potrzeb pacjenta. Ponadto doustne suplementy pokarmowe są wolne od cholesterolu, puryn i glutenu. Tylko niewielka część z nich zawiera laktozę, która może być przyczyną nietolerancji pokarmowych.
Najczęściej występujące dolegliwości, o których informują pacjenci przyjmujący ONS, to bóle brzucha, nudności i biegunki [14]. Analizując wady stosowania doustnych suplementów pokarmowych należy wskazać brak ich refundacji przez Narodowy Fundusz Zdrowia oraz wysoką cenę, która waha się od 5 zł za butelkę preparatu kompletnego do 60 zł za produkty jednoskładnikowe.
Problemy i działania uboczne związane ze stosowaniem ONS najczęściej wynikają z ich nieprawidłowego spożywania lub niewłaściwego doboru produktu.
Autorki:
dr n. med. Agata Kasprzyk1
mgr diet. Karolina Złotogórska
mgr Paulina Zegarska2
- Instytut Hematologii i Transfuzjologii w Warszawie
- Collegium Medicum, Uniwersytet Kardynała Stefana Wyszyńskiego w Warszawie
Artykuł pochodzi z 53. wydania kwartalnika Farmakoekonomika Szpitalna
Źródła:
- Sobotka L.: Podstawy żywienia klinicznego. Wyd. 4. Kraków: Krakowskie Wydawnictwo Scientifica, 2013.
- Kuhn K.S., Muscaritoli M., Wischmeyer P., Stehle P.: Glutamine as indispensable nutrient in oncology: experimental and clinical evidence. European Journal of Nutrition. 2010. Vol. 49, No. 4, 197-210.
- Kim M.-H., Kim H.: The Roles of Glutamine in the Intestine and Its Implication in Intestinal Diseases. International Journal of Molecular Science. Vol. 18, No. 5, 1051.
- Arends J., Bachmann P., Baracos V., Barthelemy N. et al.: ESPEN guidelines on nutrition in cancer patients. Clinical Nutrition. 2017. Vol. 36, No. 1, 11-48.
- Kłęk S., Kapała A.: Leczenie żywieniowe. Varia Medica. 2019. Tom 3, nr 1, 77-87.
- Serkies K.:, Pawłowska E., Jassem J.: Pooperacyjne leczenie raka trzonu macicy. Przegląd badań z losowym doborem chorych. Onkologia w praktyce klinicznej. 2013. Tom 9 , nr 6, 209-215.
- Bosaeus I., Daneryd P., Svanberg E., Lundholm K.: Dietary intake and resting energy expenditure in relation to weight loss in unselected cancer patients. International Journal of Cancer. 2001. Vol. 93, No. 3, 380-383.
- Bozzetti F., Bozzetti V.: Is the intravenous supplementation of amino acid to cancer patients adequate? A critical appraisal of literature. Clinical Nutrition. 2013. Vol. 32, No. 1, 142-146.
- Winter A., MacAdams J., Chevalier S.: Normal protein anabolic response to hyperaminoacidemia in insulin-resistant patients with lung cancer cachexia. Clinical Nutrition. Vol. 31, No. 5, 765-773.
- Van der Meij B.S., Langius J.A.E., Smit E.F., Spreeuwenberg M.D. et al.: Oral nutritional supplements containing (n-3) polyunsaturated fatty acids affect the nutritional status of patients with stage III non-small cell lung cancer during multimodality treatment. The Journal of Nutrition. 2010. Vol. 140, No. 10, 1774-1780.
- Fearon K.C.H., Von Meyenfeldt M.F., Moses A.G.W., Van Geenen R. et al.: Effect of a protein and energy dense N-3 fatty acid enriched oral supplement on loss of weight and lean tissue in cancer cachexia: a randomised double blind trial. 2003. Vol. 52, No. 10, 1479-1486.
- Kim J.M., Sung M.K.: The Efficacy of Oral Nutritional Intervention in Malnourished Cancer Patients: a Systemic Review. Clinical Nutrition Research. 2016. Vol. 5, No. 4, 219-236.
- Ravasco P., Monteiro-Grillo I., Vidal P.M., Camilo M.E.: Dietary counseling improves patient outcomes: a prospective, randomized, controlled trial in colorectal cancer patients undergoing radiotherapy. Journal of Clinical Oncology. 2005. Vol. 23, No. 7, 1431-1438.
- Kapała A.: Praktyczny przewodnik po ONS. Wyd. 1. Kraków: Krakowskie Wydawnictwo Scientifica, 2015.
- Ustawa z dnia 25 sierpnia 2006 r. o bezpieczeństwie żywności i żywienia. https://isap.sejm.gov.pl/isap.nsf/DocDetails.xsp?id=WDU20061711225 (stan z dn. 26.11.2020 r.).
Obwieszczenie Ministra Zdrowia z dnia 16 czerwca 2015 r. w sprawie ogłoszenia jednolitego tekstu rozporządzenia Ministra Zdrowia w sprawie środków spożywczych specjalnego przeznaczenia żywieniowego. www.isap.sejm.gov.pl/isap.nsf/ (stan z dn. 26.11.2020r.)